无论串连反应还是平行反应,当主反应活化能大于副反应活化能时,提高温度均有利于产物P的选择率提高。
题目
无论串连反应还是平行反应,当主反应活化能大于副反应活化能时,提高温度均有利于产物P的选择率提高。
参考答案和解析
相似问题和答案
第1题:
反应的活化能是什么?它是怎样影响化学反应速率的?为什么有些反应的活化能很接近,反应速率却相差很大、但有些反应的活化能相差较大,反应速率却很接近?
答案:反应的活化能是指化学反应中,由反应物分子到达活化分子所需的最小能量。
化学反应速率与其活化能的大小密切相关。活化能越低,反应速率越快,因此降低活化能会有效地促进反应的进行。
从碰撞理论给出的公式k=Ae-Ea/RT 可以看出,Ea以指数关系影响速率常数k值,它的确是影响反应速率的重要因素,但A也影响k值。对不同的反应,A对k的影响很大,所以活化能不是决定反应速率的唯一因素。
第2题:
对两个活化能不同的反应,当温度同样从T1升至T2时,具有活化能高的反应,其反应速率增加的倍数比活化能低的反应增加的倍数。
A、小
B、大
C、一样
第3题:
酶的催化本质是( )。
A、提高产物的能量水平
B、降低反应所需的活化能
C、降低反应物的能量水平
D、提高反应所需活化能
E、降低产物的能量水平
第4题:
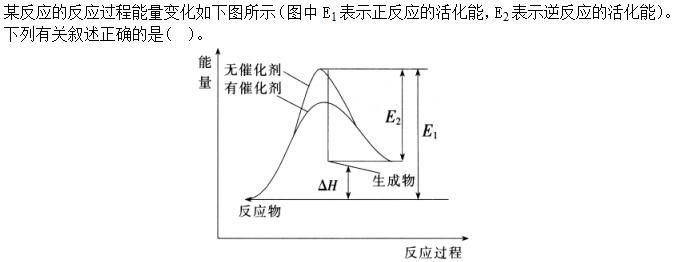
B.催化剂能改变该反应的焓变
C.催化剂能降低该反应的活化能
D.逆反应的活化能大于正反应的活化能
第5题:
B.降低反应活化能
C.使平衡发生移动
D.提高反应分子总数
第6题:
A、提高产物能量水平
B、降低反应的活化能
C、提高反应所需活化能
D、降低反应物的能量水平
第7题:
在化学反应中温度升高可以使下列哪种类型反应的速率提高的更快( )。
A.活化能高的反应
B.活化能低的反应
C.压力较高的反应
D.压力较低的反应
第8题:
A、提高反应物的活性
B、提高反应的活化能
C、降低反应的活化能
D、没有作用
第9题:
B.降低反应的活化能
C.提高反应所需活化能
D.降低反应物的能量水平
第10题:
三氧化硫磺化烷基苯具有()特点。
- A、传热快
- B、活化能高
- C、活化能低
- D、副反应少
正确答案:C
