已知一溶液只有第二组阳离子,将此溶液分成3份,分别得到下述实验结果,试判断哪些离子可能存在? (1) 用水稀释,得到白色沉淀,加HCl溶液则溶解; (2) 加入SnCl2无沉淀发生; (3) 与组试剂作用,生成黄色沉淀,此沉淀一部分溶于Na2S,另一部分不溶,仍为黄色。
题目
已知一溶液只有第二组阳离子,将此溶液分成3份,分别得到下述实验结果,试判断哪些离子可能存在? (1) 用水稀释,得到白色沉淀,加HCl溶液则溶解; (2) 加入SnCl2无沉淀发生; (3) 与组试剂作用,生成黄色沉淀,此沉淀一部分溶于Na2S,另一部分不溶,仍为黄色。
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
实验室现有四瓶失去标签的蔗糖溶液(编号A、B、C、D),已知四瓶蔗糖溶液的浓度都不同。现利用半透膜袋进行渗透实验(装置如下图),一段时间后半透膜袋①和③变得胀硬,半透膜袋②萎缩。四种蔗糖溶液中浓度最低的是( )。


A.蔗糖溶液A
B.蔗糖溶液B
C.蔗糖溶液C
D.蔗糖溶液D
B.蔗糖溶液B
C.蔗糖溶液C
D.蔗糖溶液D
答案:B
解析:
【知识点】本题考查渗透作用。 【答案】B。
【解析】根据水分从低浓度向高浓度扩散的原理,半透膜袋①和③变得胀硬,说明浓度A>D,C>D;半透膜袋②萎缩,说明浓度D>B。所以,浓度最小的是B。
【解析】根据水分从低浓度向高浓度扩散的原理,半透膜袋①和③变得胀硬,说明浓度A>D,C>D;半透膜袋②萎缩,说明浓度D>B。所以,浓度最小的是B。
第2题:
实验室内部评价检验方法的精密度和准确度时,哪组溶液最好每天同时测定()。
- A、空白溶液和样品溶液
- B、空白溶液、标准溶液、样品溶液和加标样品溶液
- C、标准溶液和样品溶液
- D、空白溶液、标准溶液和样品溶液
- E、空白溶液和加标样晶溶液
正确答案:B
第3题:
把浓度为20%、30%和50%的某溶液混合在一起,得到浓度为36%的溶液50升。已知浓度为30%的溶液用量是浓度为20%的溶液用量的2倍,浓度为30%的溶液的用量是多少升
A.18 B.8 C.10 D.20
A.18 B.8 C.10 D.20
答案:D
解析:

第4题:
已知三元弱酸的三级电离常数分别为:Ka1=1×10-3,Ka2=1×10-5,Ka3=1×10-6。 将此酸配成溶液后,用NaOH标准滴定溶液滴定时,应有()个pH突跃,宜选用()为指示剂。
正确答案:1;酚酞
第5题:
有一种黑色的固体铁的化合物(A),溶于盐酸时,可得到浅绿色溶液(B),同时放出有臭味的气体(C),将此气体导入硫酸铜溶液中得到黑色沉淀(D),若将Cl2气通入B溶液中则溶液变成棕黄色(E),再加硫氰化钾溶液变成血红色(F),问:(A),(B),(C),(D),(E),(F)各为何物?并写出有关化学方程式.
正确答案: AFeSB:FeCl2C://H2S
DCuSE://FeCl3F://〔Fe(NCS)n〕3-
FeS+2HCl==FeCl2+H2S↑
CuSO4+H2S==CuS↓+H2SO4
2FeCl2+Cl2==2FeCl3
Fe3++nSCN-==〔Fe(SCN)n〕3-
第6题:
蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是()
- A、沉淀X的成分是SiO2
- B、将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3
- C、在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
- D、溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
正确答案:B
第7题:
根据实验现象写出方程式当黄色BaCrO4沉淀溶解在浓HCl溶液中时得到一个绿色溶液
正确答案: 2BaCrO4+4HCl=2BaCl2+H2Cr2O7+H2O
H2Cr2O7+12HCl=2CrCl3+3Cl2↑+7H2O
__________________________________________
2BaCrO4+16HCl=2BaCl2+8H2O+3Cl2↑+2CrCl3
Cr(Ⅲ)的配离子[Cr(H2O)4Cl2]+绿色
第8题:
某初中化学教师在一次测验中设计了下列试题.并对部分学生的解题结果进行了统计和分析。
【试题】实验室现有3瓶失去标签的无色溶液。已知它们分别是NaN03、NaCl、Na2C03的溶液,请设计实验方案,将它们一一鉴别。
【考试结果】有30%N学生提交了下面的方案:分别取三种溶液样品少量,放入三支试管中,向三支试管各滴入稀盐酸,有气泡冒出的溶液是Na2C03溶液,再向无明显现象的两支试管里分别滴AgN03溶液,有白色沉淀产生的原溶液是NaCl溶液,无明显现象的原溶液是NaN03溶液。
根据上述信息,回答:
(1)请设计出本实验正确的鉴别方案。
(2)试对上述学生答题错误的原因进行分析。
(3)写出本实验中涉及的有关化学反应方程式。
【试题】实验室现有3瓶失去标签的无色溶液。已知它们分别是NaN03、NaCl、Na2C03的溶液,请设计实验方案,将它们一一鉴别。
【考试结果】有30%N学生提交了下面的方案:分别取三种溶液样品少量,放入三支试管中,向三支试管各滴入稀盐酸,有气泡冒出的溶液是Na2C03溶液,再向无明显现象的两支试管里分别滴AgN03溶液,有白色沉淀产生的原溶液是NaCl溶液,无明显现象的原溶液是NaN03溶液。
根据上述信息,回答:
(1)请设计出本实验正确的鉴别方案。
(2)试对上述学生答题错误的原因进行分析。
(3)写出本实验中涉及的有关化学反应方程式。
答案:
解析:
(1)方案为在三种溶液加入过量稀硝酸溶液,产生气泡的原溶液为碳酸钠溶液。在剩余两种溶液中滴加少量硝酸银溶液,产生白色沉淀的原溶液为氯化钠溶液,无现象的原溶液为硝酸钠溶液。 (2)学生的失误在于第一步鉴别碳酸钠溶液时加入盐酸.引入氯离子,从而使剩余两种溶液在滴加硝酸银溶液时均会产生白色溶液.导致剩余两种溶液不能鉴别.
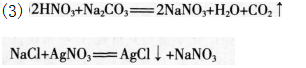
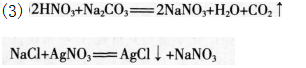
第9题:
在常温下,将同一NaOH溶液滴入CdSO4和HgSO4溶液中,分别得到()、()
正确答案:Cd(OH)2;HgO
第10题:
分别用1mol/L的硝酸银溶液10ml与相同体积的下述溶液恰好完全反应,下述溶液中摩尔浓度最小的是()。
- A、氯化钠溶液
- B、氯化钾溶液
- C、氯化钙溶液
- D、氯化铁溶液
正确答案:D
