同一个反应在相同反应条件下未加催化剂时平衡常数及活化能为k及Ea,加入正催化剂后则为k'、Ea',则存在下述关系:()A、k'=k,Ea=Ea'B、k'≠k,Ea≠Ea'C、k'=k,Ea>Ea'D、k<k,Ea'<Ea
题目
同一个反应在相同反应条件下未加催化剂时平衡常数及活化能为k及Ea,加入正催化剂后则为k'、Ea',则存在下述关系:()
- A、k'=k,Ea=Ea'
- B、k'≠k,Ea≠Ea'
- C、k'=k,Ea>Ea'
- D、k<k,Ea'<Ea
参考答案和解析
正确答案:C
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
在1133K时于一恒容容器中发生如下反应:
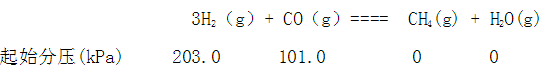
平衡时CH4的分压为13.2kPa,求该反应在1133K时的平衡常数Kc及各物质的平衡浓度。
参考答案:

第2题:
催化剂可加快反应速率的原因。下列叙述正确的是:

C.降低了反应的活化能
D.使反应的平衡常数Kθ减小

C.降低了反应的活化能
D.使反应的平衡常数Kθ减小
答案:C
解析:
提示 催化剂之所以加快反应的速率,是因为它改变了反应的历程,降低了反应的活化能,增加了活化分子百分数。
第3题:
在可逆反应中加入催化剂,下列叙述不正确的是()
A.改变了反应的ΔrHm
B.改变了反应的ΔrGm
C.改变了正逆反应的活化能,但改变量ΔEa不同
D.改变了正逆反应的活化能,但改变量ΔEa相同
参考答案:ABC
第4题:
在化学反应中,催化剂的作用在于()
- A、降低反应活化能
- B、增加反应活化能
- C、增大反应的平衡常数
- D、增大正向反应速率
正确答案:A
第5题:
某一级反应的半衰期在300 K时为50 min,在310 K时为10 min,则该反应的活化Ea=()kJ·mol-1。
A.14.97
B.-124.43
C.124.43
D.-14.97
B.-124.43
C.124.43
D.-14.97
答案:C
解析:
第6题:
已知在相同条件下,下列反应的平衡常数为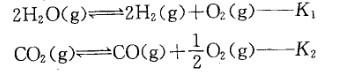
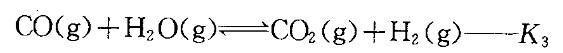
则K3与K2、K1的关系为:
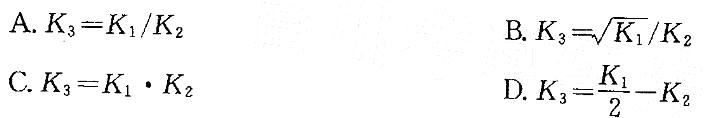
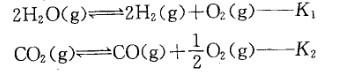
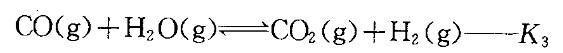
则K3与K2、K1的关系为:
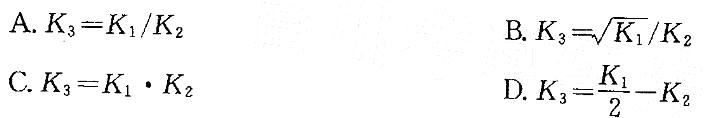
答案:B
解析:
提示:当n个反应相加(或相减)得总反应时,总反应的平衡常数等于各个反应平衡常数的乘积(或商)。
第7题:
在800K下,I2(g)作为催化剂加速气相乙醛分解反应,其反应为CH3CHO(g)
一→ CH4(g)+ CO(g),若无催化剂存在时,分解反应的活化能为190.38 kJ·mol~-1,当加入催化剂后,在同样条件下,反应速率增至原速率的3600倍,则催化剂加人后,反应活化能降低了
()kJ.mol-1。(设指前因子A不变)
一→ CH4(g)+ CO(g),若无催化剂存在时,分解反应的活化能为190.38 kJ·mol~-1,当加入催化剂后,在同样条件下,反应速率增至原速率的3600倍,则催化剂加人后,反应活化能降低了
()kJ.mol-1。(设指前因子A不变)
A.54.4
B.6.55
C.0.0068
D.数据不足,无法计算
B.6.55
C.0.0068
D.数据不足,无法计算
答案:A
解析:
第8题:
根据阿仑尼乌斯公式,对不同反应, 升高相同温度, 活化能Ea大的反应速率常数k增加的倍数大。()
此题为判断题(对,错)。
参考答案:正确
第9题:
加入催化剂能()。
- A、改变反应历程
- B、增大平衡常数K值
- C、提高反应活化能
正确答案:A
第10题:
反应A+B=AB的活化能是Ea,加入催化剂K后,反应历程发生变化,A+K=AK,活化能为E1,AK+B=AB+K,活化能为E2,(Ea>E2>E1)则加入催化剂后,反应的活化能为()
- A、E1
- B、E2
- C、E1+E2
- D、E1-E2
正确答案:B
