根据晶体场理论,在一个八面体强场中,中心离子d电子数为()时,晶体场稳定化能最大。A、9B、6C、5D、3
题目
根据晶体场理论,在一个八面体强场中,中心离子d电子数为()时,晶体场稳定化能最大。
- A、9
- B、6
- C、5
- D、3
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
连接正方体每个面的中心构成一个正八面体(如下图所示)。已知正方体的边长为6厘米,问正八面
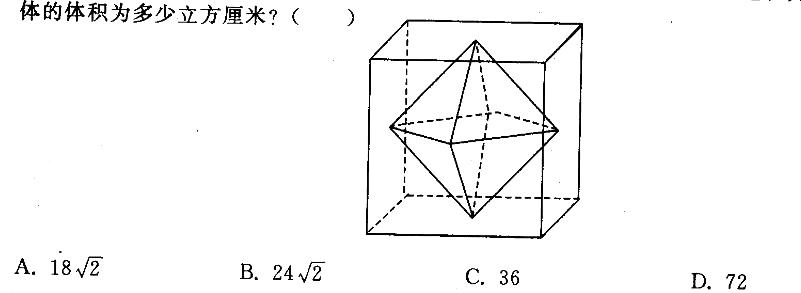

答案:C
解析:
该正八面体可以看做由两个四棱锥拼成的,每个四棱锥的底面为原正方体四个侧面的中心连线,高分别为上下两个正方体底面中心到四棱锥底面的距离,解得V= 1/3x(62x1/2)X3X2 =36(cm3)。
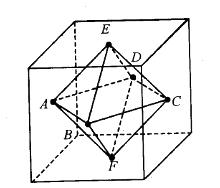

第2题:
体心立方结构每个晶胞中八面体间隙数为()。
A.4
B.6
C.8
D.12
B.6
C.8
D.12
答案:B
解析:
第3题:
在晶体场理论中,在八面体场中Oh场作用下d轨道分裂为()和()。
A、e,t2g
B、eg,tg
C、e,t2
D、eg,t2g
参考答案:D
第4题:
当ΔO>P时,过渡金属离子能形成()自旋八面体配合物;当ΔO<P时,则形成()自旋八面体配合物;前者的CFSE与P()关。
正确答案:低;高;有
第5题:
解释宝石颜色的形成机理的晶体场理论是描述:()
- A、离子外层电子跃迁
- B、晶体的能带
- C、离子与配位体的静电作用
- D、分子的化学键
正确答案:A,C
第6题:
连接正方体每个面的中心构成一个正八面体(如下图所示)。已知正方体的边长为6厘 米,问正八面体的体积为多少立方厘米?( )
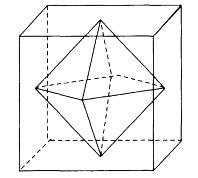



答案:C
解析:

第7题:
已知H2O为弱场配体,CN-为强场配体。利用晶体场理论说明[Fe(H2O)6]3+和[Fe(CN)6]3–是低自旋配合物还是高自旋配合物,并写出中心原子的d电子排布。
正确答案: H2O为弱场配体,
第8题:
在八面体场中,既能形成低自旋又能形成高自旋配合物的过渡元素的d电子数应为()。
A.1~3个
B.2~5个
C.4~6个
D.6~9个
标准答案:C
第9题:
连接正方体每个面的中心构成一个正八面体。己知正方体的边长为6厘米,问正八面体的体积为多少立方厘米?()
- A、182
- B、242
- C、36
- D、72
正确答案:C
第10题:
某金属离子在八面体强场中的磁矩与在八面体弱场中的磁矩几乎相等,则该离子可能是()
- A、Mn2+
- B、Cr3+
- C、Mn3+
- D、Fe3+
正确答案:B
