金属铜不镕于稀盐酸,但在硫脲存在下,铜与浓盐酸反应产生氢气。这是由于生成(),而使铜的()增强的缘故。铜与HI溶液反应生成H2和白色的()沉淀。
题目
金属铜不镕于稀盐酸,但在硫脲存在下,铜与浓盐酸反应产生氢气。这是由于生成(),而使铜的()增强的缘故。铜与HI溶液反应生成H2和白色的()沉淀。
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
稀硝酸与铜的反应产物不同于浓硝酸与铜的反应产物。()
此题为判断题(对,错)。
参考答案:正确
第2题:
如图所示,天平左右两端的烧杯中有等量稀盐酸,并处于平衡状态。现在天平左右两端的烧杯中,分别加入相同质量的锌块与铜块,结果发现天平右侧缓慢下降,主要的原因是( )。
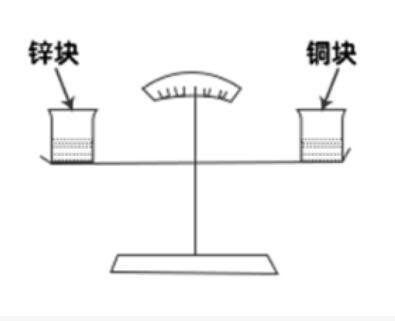

A.相同质量的铜块与锌块大小不同
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
B.铜块与稀盐酸反应产生了氯化铜
C.锌块与稀盐酸反应产生了氢气
D.化学反应产生了大量水蒸气
答案:C
解析:
第一步,确定题型。
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
本题考查化学反应。
第二步,根据天平的状态进行分析。
①初始:天平两端有等量稀盐酸,并处于平衡状态。
②过程:相同质量的锌块与铜块分别加入天平左右两端。
③结果:天平右侧(铜块)缓慢下降。
第三步,分析选项。
A项:天平是称质量的,整体的上升和下降只与物体的质量有关系,与体积没有关系,排除;
B项:铜块与稀盐酸不反应,排除;
C项:锌块和稀盐酸反应产生了氢气,质量变轻,符合;
D项:铜块不与稀盐酸发生反应,锌块和稀盐酸反应产生氢气,不是水蒸气,排除。
因此,选择C选项。
第3题:
硝酸和硫酸共有的性质是()。
A、浓酸或稀酸能把铜氧化
B、都有吸水性
C、稀酸都能跟活泼的金属反应放出氢气
D、冷的浓酸使铁、铝钝化
参考答案:D
第4题:
测量一定质量的铝锌合金与强酸溶液反应产生氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学实验常用仪器、800mL烧杯、100mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19g/cm3)、水.合金样品用铜网包裹的目的是什么?
正确答案:使样品在反应时能在烧杯底适当的位置(或答避免反应时样品漂浮).
第5题:
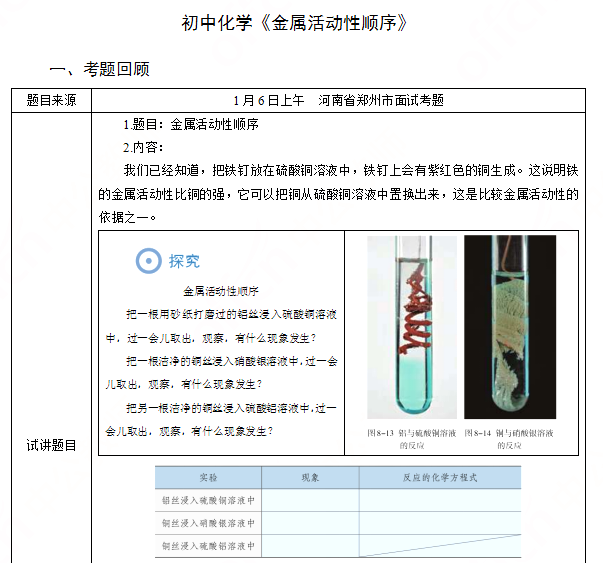


【学生回答】锌与硫酸生成氢气和硫酸锌。通过上节课的实验可以知道铜与硫酸不发生反应。
【教师引导】既然锌能与酸反应,铜不能与酸反应,由此可知金属的活泼性是不同的。那么金属的活动性强弱是怎样的顺序呢,这节课我们就一起来探究金属的活动性。
(二)新课讲授
【学生实验】①铁与硫酸铜的反应;②铁、铜分别与盐酸的反应
【提出问题】通过实验,思考铁与铜,哪种金属更加活泼?为什么?
【学生回答】铁比铜活泼,因为铁与盐酸发生了反应,有气泡产生,而铜与盐酸不反应,并且铁能把铜从硫酸铜溶液中置换出来,说明铁更活泼。
【提出问题】通过这两组实验,你能说说我们在证明金属活动性强弱时采取的实验方法吗?
【学生回答】第一种方法是让金属与另一金属的盐溶液反应,根据能否发生置换反应判断金属活泼性强弱;第二种方法是让金属与酸反应,根据能否发生反应、发生反应的剧烈程度来判断金属活泼性强弱。
【教师引导】现有镁、铜、锌三种金属,利用上述实验方法,你能设计方案并通过实验来判断镁、铜、锌三种金属谁的活动性更强吗?
(药品:镁条、铜丝、锌粒、稀盐酸、稀硫酸、氯化镁溶液、硫酸锌溶液、硫酸铜溶液。)
(小组讨论5分钟)
【提出问题】哪个小组愿意说一下自己小组的实验方案?
【学生回答】
小组①:将镁条、铜丝、锌粒分别与稀盐酸反应,观察反应的剧烈程度来判断活动性强弱。

【提出问题】根据金属活动性顺序表来看,金属所处的位置与活泼性有什么关系?排在H前面的金属有什么特点?排在前面的金属与后面金属的盐溶液能否发生反应?
【学生回答】
(1)在金属活泼性顺序里,金属的位置越靠前,它的活泼性就越强;
(2)在金属活泼性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢;
(3)在金属活泼性顺序里,位于前面的金属能把位于后面的金属从其盐溶液中置换出来。
(三)巩固提高
请根据金属活动性顺序表判断下列反应能否发生?
(1)铁和稀盐酸
(2)铝和硫酸锌溶液
(3)铁与硫酸铜晶体
解析:(1)反应;(2)反应;(3)不反应
(四)小结作业
请学生回答本堂课的收获:金属活动性顺序。
布置作业:有一种“黄铜”又称为“愚人金”,实为铜、锌合金。“黄铜”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。能不能利用所学知识,设计实验来鉴别金与“愚人金”?
【板书设计】

【答辩题目解析】
1.铝的化学性质很活泼,为什么通常铝制品却很耐腐蚀?为什么不宜用钢刷、沙等来擦洗铝制品?
2.请谈一谈你这样设计导入的原因?
答案:
解析:
1.
铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止铝进一步氧化,因此,铝制品具有耐腐蚀性。如果用钢刷、沙等来擦洗铝制品,很容易破坏铝制品表面致密的氧化铝薄膜。
2.
导入我采用的是通过大屏幕出示三个置换反应的反应物,让学生来判断产物。学生根据上节课做过的实验能够准确地得出结论,由此引出金属具有不同的活泼性,从而进入本节课的学习。采用这种复习的导入方法既可以检测学生对上节课置换反应内容的掌握程度,又可以降低学习新知识的难度,帮助学生克服心理上的恐惧,使学生在学习新内容时既有了思想准备,又有了知识基础,学习起来轻松自如。
铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止铝进一步氧化,因此,铝制品具有耐腐蚀性。如果用钢刷、沙等来擦洗铝制品,很容易破坏铝制品表面致密的氧化铝薄膜。
2.
导入我采用的是通过大屏幕出示三个置换反应的反应物,让学生来判断产物。学生根据上节课做过的实验能够准确地得出结论,由此引出金属具有不同的活泼性,从而进入本节课的学习。采用这种复习的导入方法既可以检测学生对上节课置换反应内容的掌握程度,又可以降低学习新知识的难度,帮助学生克服心理上的恐惧,使学生在学习新内容时既有了思想准备,又有了知识基础,学习起来轻松自如。
第6题:
下列物质能否发生反应?写出能发生反应的化学方程式。
(1)银与稀盐酸 (2)锌与硫酸铜溶液
(3)铜与硫酸锌溶液 (4)铝与硝酸银溶液
(1)不反应
(2)Zn+CuSO4=ZnSO4+Cu
(3)不反应
(4)Al+3AgNO3=Al(NO3)3+3Ag
第7题:
下列有关金属的说法错误的是( )
A.铜能导电
B.银能与稀盐酸反应
C.镁的活动性比铁强
D.铝具有良好的抗腐蚀性
B.银能与稀盐酸反应
C.镁的活动性比铁强
D.铝具有良好的抗腐蚀性
答案:B
解析:
A、铜具有优良的导电性,能导电,故选项说法正确.
B、银的金属活动性比氢弱,不能与稀盐酸反应,故选项说法错误.
C、在金属活动性顺序中,镁排在铁的前面,镁的活动性比铁强,故选项说法正确.
D、铝的表面有一层致密的氧化铝薄膜,铝具有良好的抗腐蚀性,故选项说法正确.
故选:B.
B、银的金属活动性比氢弱,不能与稀盐酸反应,故选项说法错误.
C、在金属活动性顺序中,镁排在铁的前面,镁的活动性比铁强,故选项说法正确.
D、铝的表面有一层致密的氧化铝薄膜,铝具有良好的抗腐蚀性,故选项说法正确.
故选:B.
第8题:
既能跟盐酸,又能跟氢氧化钠反应,产生氢气的物质是( )。
A.铝
B.铁
C.铜
D.氧化铝
正确答案:A
第9题:
镁、铁、铝、铜都能与稀盐酸反应放出氢气。()
正确答案:错误
第10题:
稀硝酸与铜的反应产物不同于浓硝酸与铜的反应产物。
正确答案:正确
