把A、B、C三种金属片分别加入稀硫酸中,A、B表面有气泡产生,C无变化;把A加入B的硫酸盐溶液中,A表面析出B。则这三种金属的活动性顺序为()A、B>A>CB、A>B>CC、C>B>AD、A>C>B
题目
把A、B、C三种金属片分别加入稀硫酸中,A、B表面有气泡产生,C无变化;把A加入B的硫酸盐溶液中,A表面析出B。则这三种金属的活动性顺序为()
- A、B>A>C
- B、A>B>C
- C、C>B>A
- D、A>C>B
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
下列加入的物质起催化作用的是( )
A.电解水时,加入少量KOH,电解速率加快
B.Zn与稀硫酸反应时,加入几滴CuS04溶液,产生H2速率加快
C.皂化反应后,加入食盐细粒,加快肥皂析出
D.双氧水中加入Mn02粉末,产生气泡明显增多
B.Zn与稀硫酸反应时,加入几滴CuS04溶液,产生H2速率加快
C.皂化反应后,加入食盐细粒,加快肥皂析出
D.双氧水中加入Mn02粉末,产生气泡明显增多
答案:D
解析:
第2题:
将纯锌片和纯铜片按图3所示方式插入同浓度的稀硫酸中,下列叙述正确的是( )。
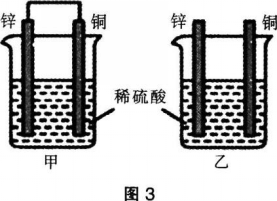

A.两烧杯中铜片表面均无气泡产生
B.甲中铜片是阳极.锌片是阴极
C.一段时间后两烧杯中溶液的pH均增大
D.甲产生气泡的速度比乙慢
B.甲中铜片是阳极.锌片是阴极
C.一段时间后两烧杯中溶液的pH均增大
D.甲产生气泡的速度比乙慢
答案:C
解析:
甲可形成原电池,锌片为负极,铜片为正极,在正极处氢离子得电子产生氢气,有气泡产生。A、B两项错误。甲、乙均消耗稀硫酸,放出氢气,故氢离子浓度均减小,pH增大,C项正确。原电池能加快氧化还原反应的速率,因此甲产生气泡的速度比乙快,D项错误。
第3题:
②以铝材为阳极,在H2SO4溶液中电解,铝材表面形成氧化膜,阳极电极反应式为______________。取少量废电解液,加入NaHCO3溶液后产生气泡和白色沉淀,产生沉淀的原因是__________________。
正确答案:
②2Al+3H2O=Al2O3+6H++6e-;
HCO3-与H+反应使H+浓度减小,产生Al(OH)3沉淀。(合理即得分)
第4题:
用98%的浓硫酸配制成稀硫酸应()。
- A、将硫酸加入水中
- B、将水加入硫酸中
- C、与操作程序无关
正确答案:A
第5题:
在甲、乙试管中各加入2mL体积分数为30%的过氧化氢溶液,再向甲试管中加入2滴新鲜动物肝脏匀浆,向乙试管中加入2滴质量分数为3.5%的溶液,观察到的现象是( )。
A.甲试管比乙试管产生气泡的速率快
B.甲试管比乙试管产生气泡的速率慢
C.甲试管不产生气泡,乙试管产生气泡
D.甲试管产生气泡,乙试管不产生气泡
B.甲试管比乙试管产生气泡的速率慢
C.甲试管不产生气泡,乙试管产生气泡
D.甲试管产生气泡,乙试管不产生气泡
答案:A
解析:
知识点:酶的高效性。溶液与新鲜动物肝脏匀浆中的过氧化氢酶都能催化过氧化氢释放氧气,产生气泡,酶的催化效率比无机催化剂高,所以甲试管比乙试管产生气泡的速率快。因此答案选A。
第6题:
在沸腾换热过程中,产生的气泡不断脱离表面,形成强烈的对流换热,其中,产生的气泡能够存在并能继续长大的条件( )。
A.
B.
C.
D.壁面处有气化核心

B.

C.

D.壁面处有气化核心
答案:B
解析:

第7题:
由C、CuO、Fe三种物质组成的混合物,放在试管中,如图所示高温加热。
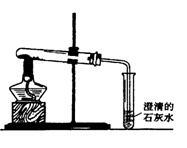
当观祭到澄清石灰水变浑浊时,停止加热,密封冷却至室温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红色物质明显增加。请根据这些信息,推断红色物质增加的可能的原因(用化学万程式表) ( )、( )

当观祭到澄清石灰水变浑浊时,停止加热,密封冷却至室温;然后往试管中加入稀硫酸,观察到有气泡冒出,且红色物质明显增加。请根据这些信息,推断红色物质增加的可能的原因(用化学万程式表) ( )、( )
答案:
解析:
CuO+H2SO4 =CuSO4+H2O CuSO4+Fe=FeSO4+Cu
第8题:
现有X、Y、Z三种金属,如果把X和Y分别放入稀硫酸中,X溶解并产氢气,Y不反应;如果把Y和Z分别放入硝酸银溶液中,过一会儿,在Y表面有银析出,而Z没有变化。根据以上实验事实,判断X、Y、Z的金属活动性顺序。
X>Y>Z
第9题:
鉴定草酸钙结晶的方法有
A.加稀醋酸溶解
B.加稀醋酸不溶解,加稀盐酸溶解而无气泡产生
C.加硫酸溶液逐渐溶解,片刻后析出针状结晶
D.加稀硫酸溶液不溶解
E.加稀盐酸溶解,同时有气泡产生
B.加稀醋酸不溶解,加稀盐酸溶解而无气泡产生
C.加硫酸溶液逐渐溶解,片刻后析出针状结晶
D.加稀硫酸溶液不溶解
E.加稀盐酸溶解,同时有气泡产生
答案:B,C
解析:
本题考查草酸钙的鉴定方法。草酸钙结晶在装片时加入硫酸溶液逐渐溶解,并析出针状硫酸钙结晶,以此与硅酸盐相区别;加入稀盐酸溶解,但没有气泡产生,可与碳酸盐相区别。
第10题:
二沉池表面正常情况下允许有少量气泡产生。
正确答案:正确
