将15.0g糖(C6H12O6)溶于200g水中。该溶液的冰点(kfp=1.86)是:()A、-0.258℃B、-0.776℃C、-0.534℃D、-0.687℃
题目
将15.0g糖(C6H12O6)溶于200g水中。该溶液的冰点(kfp=1.86)是:()
- A、-0.258℃
- B、-0.776℃
- C、-0.534℃
- D、-0.687℃
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
将15.0g糖(C6H12O6)溶于200g水中。该溶液的冰点(kfp=1.86)是:
A. -0. 258°
B. -0. 776°
C. -0. 534°
D. -0. 687°
B. -0. 776°
C. -0. 534°
D. -0. 687°
答案:B
解析:
提示:ΔTfp=Kfp . m ,注意式中m为质量摩尔浓度。
第2题:
在20°C时,将7.50g葡萄糖(C6H1206)溶于100g水中。该溶液的渗透压为:
A. 69. 3Pa
B. 1. 02X103kPa
C. 1.02X103Pa
D. 69. 3kPa
B. 1. 02X103kPa
C. 1.02X103Pa
D. 69. 3kPa
答案:C
解析: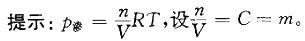
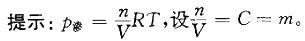
第3题:
将固体NH4NO3溶于水中,溶液变冷,则该过程的ΔG<0,ΔH<0,ΔS>0()
此题为判断题(对,错)。
参考答案:错误
第4题:
将15.0g糖(C3H12O3)溶于200g水中。该溶液的冰点(kfp=1.86)是()
- A、-0.258℃
- B、-0.776℃
- C、-0.534℃
- D、-0.687℃
正确答案:B
第5题:
将15.0g糖(C6H12O6)溶于200g水中。该溶液的冰点(kfp=1.86)是:
A. -0. 258°C B. -0. 776°C C. -0. 534°C D. -0. 687°C
A. -0. 258°C B. -0. 776°C C. -0. 534°C D. -0. 687°C
答案:B
解析:
提示:ΔTfp=Kfp . m ,注意式中m为质量摩尔浓度。
第6题:
2.76g甘油溶于200g水中得到一种溶液,测得该溶液的凝固点为-0.279℃,水的Kfp=1.86K·kg/mol。据此求出该甘油的摩尔质量是( )。
A.860g/mol
B.920g/mol
C.900g/mol
D.940g/mol
B.920g/mol
C.900g/mol
D.940g/mol
答案:B
解析:
根据公式Kfp·m=△Tfp进行计算
第7题:
在20℃时,将15.0g葡萄糖(C6H12O6)溶于200g水中,该溶液的冰点(Kfp=1.86℃)、正常沸点(Kbp=0.52℃)、渗透压(设M=m)分别是( )。

答案:C
解析:

第8题:
在实验室中配制SnCl2溶液,并要求该溶液能在较长时间内使用,宜采用如下何种方法:( )。
A.将SnCl2溶于加有适量HCL的纯水中
B.将SnCl2溶于加有适量HCL的纯水中,并加入少量锡粒
C.将SnCl2溶于加有少量Na2CO3的纯水中
正确答案:B
第9题:
纯碱溶于水中溶液呈()性。
正确答案:碱
第10题:
糖的浓度越高,溶液冰点下降的越小。
正确答案:错误
