单选题相同温度下等物质的量浓度的下列溶液中,pH值最小的是()A NH4ClB NH4HCO3C NH4HSO4D (NH4)2SO4
题目
单选题
相同温度下等物质的量浓度的下列溶液中,pH值最小的是()
A
NH4Cl
B
NH4HCO3
C
NH4HSO4
D
(NH4)2SO4
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
物质的量浓度相同的下列溶液, pH最大的是()
A.FeCl 3
B.Na 2 S
C.NaCl
D.CH 3 COOH
参考答案:B
第2题:
相同温度下,物质的量浓度均为0.1?mol/L的下列各溶液:?
请按pH由小到大的顺序排列( )。

请按pH由小到大的顺序排列( )。
A、④②③①⑤
B、③④②⑤①
C、⑤①②③④
D、②⑤①③④
B、③④②⑤①
C、⑤①②③④
D、②⑤①③④
答案:A
解析:
题干所述五种物质均为强碱弱酸盐,所以都呈碱性。要比较它们的pH,也就是要比较它们的碱性强弱。强碱弱酸盐所对应的酸的酸性越强,则形成的强碱弱酸盐的碱性越弱。因为酸性:醋酸>碳酸>苯酚>碳酸氢根>偏铝酸,故碱性:醋酸钠<碳酸氢钠<苯酚钠<碳酸钠<偏铝酸钠。
第3题:
物质的量相同的下列物质的水溶液,其pH值最高的是()
A、NaAc
B、Na2CO3
C、NH4Cl
D、NH4Ac
参考答案:B
第4题:
物质的量浓度(以化学式为基本单元)相同的情况下,下列物质的水溶液pH值最高的是()。
- A、NaAc
- B、Na2CO3
- C、NH4CL
- D、NaCL
- E、NH4Ac
正确答案:B
第5题:
下列同浓度的物质溶液中,pH值最大的是()
- A、NH4Ac
- B、NaCN
- C、NaAc
- D、HCN
正确答案:C
第6题:
用同一NaOH溶液,分别与相同体积的盐酸、醋酸溶液反应,完全反应后消耗了相同量的NaOH溶液.由此说明该盐酸和醋酸溶液的关系是( )
A.H+浓度相同
B.物质的量浓度相同
C.溶质的质量分数相同
D.pH相同
B.物质的量浓度相同
C.溶质的质量分数相同
D.pH相同
答案:B
解析:
【解题指要】 (1)首先应明确盐酸、醋酸溶液分别与NaOH溶液反应,消耗NaOH溶液的量与盐酸、醋酸溶液中所含溶质的量成正比. 从反应方程式中可知它们的质量比和物质的量之比.

由此可知,若消耗NaOH溶液的量相等,则盐酸、醋酸溶液中所含溶质的物质的量一定相等,但质量一定不等,即n(HCl)=n(CH3COOH),m(HCl)≠m(CH3COOH).

质的量浓度相等.故B选项正确.
因不知溶液的总质量,所以溶质的质量分数一般不同,即C选项错误.
(2)其次,应知道盐酸是强酸,醋酸是弱酸,它们的电离程度不同.
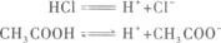
当HCl、CH3COOH的物质的量相同时,溶液中H+的物质的量一定不同,即H+的物质的量浓度一定不同.所以A选项错误.
(3)根据pH=-lg c(H+)可知,H+浓度不同,溶液的pH也一定不同,即溶液的酸性强弱不同.所以D选项也错误.

由此可知,若消耗NaOH溶液的量相等,则盐酸、醋酸溶液中所含溶质的物质的量一定相等,但质量一定不等,即n(HCl)=n(CH3COOH),m(HCl)≠m(CH3COOH).

质的量浓度相等.故B选项正确.
因不知溶液的总质量,所以溶质的质量分数一般不同,即C选项错误.
(2)其次,应知道盐酸是强酸,醋酸是弱酸,它们的电离程度不同.
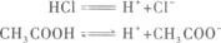
当HCl、CH3COOH的物质的量相同时,溶液中H+的物质的量一定不同,即H+的物质的量浓度一定不同.所以A选项错误.
(3)根据pH=-lg c(H+)可知,H+浓度不同,溶液的pH也一定不同,即溶液的酸性强弱不同.所以D选项也错误.
第7题:
下列比较中,正确的是()。
A.同温和同物质的量浓度时,HF比HCN易电离,则溶液pH:NaF>NaCN
B.物质的量浓度相等的H2S和NaHS混合溶液中: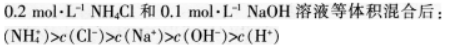
C.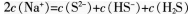
D.将①0.01mol·L-1的CH3COOH溶液;②0.01mol·L-1的盐酸;③pH=12的氨水;④pH=12的NaOH溶液稀释相同倍数后溶液的pH:③>④>②>①
B.物质的量浓度相等的H2S和NaHS混合溶液中:
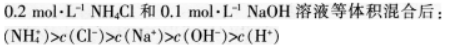
C.
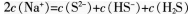
D.将①0.01mol·L-1的CH3COOH溶液;②0.01mol·L-1的盐酸;③pH=12的氨水;④pH=12的NaOH溶液稀释相同倍数后溶液的pH:③>④>②>①
答案:B
解析:
同温和同物质的量浓度时,HF比HCN易电离,这说明HF的酸性强于HCN,酸性越弱,相应的钠盐越容易水解.所得溶液碱性越强.DH越大.则溶液DH:NaF<NaCN.A项错误:根据物料守恒可知,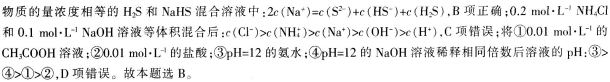
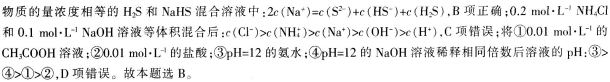
第8题:
物质的量浓度相同的下列物质的水溶液,其pH值最高的是( )
A.Na2CO3
B.NaAc
C.NH4Cl
D.NaCl
正确答案:A
第9题:
关于盐酸与醋酸两种稀溶液的说法错误的是()。
- A、相同浓度的两种溶液中相同
- B、100毫升0.1摩尔每升的两溶液能中和等物质的量的氢氧化钠
- C、pH为3的两溶液稀释100倍,pH均为5
- D、两溶液中分别加入少量对应的钠盐,氢离子的物质的量浓度明显减少
正确答案:A,C,D
第10题:
在下列选项中,()对HPAM(聚丙烯酰胺)溶液的粘度影响不大。
- A、PH值
- B、聚合物分子量
- C、温度
- D、聚合物溶液浓度
正确答案:A
