多选题在配置NaOH溶液时,()使所配溶液的物质的量浓度偏低。A在容量瓶中加入,使溶液凹液面与刻度线相切BNaOH颗粒表面部分变质C未将烧杯的洗液注入容量瓶D容量瓶使用前蒸馏水洗过
题目
多选题
在配置NaOH溶液时,()使所配溶液的物质的量浓度偏低。
A
在容量瓶中加入,使溶液凹液面与刻度线相切
B
NaOH颗粒表面部分变质
C
未将烧杯的洗液注入容量瓶
D
容量瓶使用前蒸馏水洗过
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
配制一定物质的量浓度的氢氧化钠溶液时,造成所配溶液浓度偏高的原因是( )。
A.所用NaOH已潮解
B.有少量的NaOH溶液残留在烧杯里
C.向容量瓶中加水超过刻度线
D.容量瓶使用前,用NaOH溶液润洗过
参考答案:D
第2题:
已知某标准NaOH溶液在保存中吸收了少量CO2,用此溶液来标定盐酸溶液,若以酚酞作指示剂,则使盐酸溶液的浓度标定结果()。
A、偏低;
B、偏高;
C、无影响;
D、无法确定。
参考答案: B
第3题:
配置一定物质的量浓度的氢氧化钠溶液时,洗涤液转入容量瓶时,不慎倒在瓶外,使配置溶液的浓度偏高。()
此题为判断题(对,错)。
参考答案:错误
第4题:
在配制NaOH溶液时,会使溶液物质的量浓度产生偏低现象的是()。
- A、往容量瓶中加入,使溶液凹液面与刻度线相切
- B、NaOH颗粒表面部分变质
- C、未将烧杯的洗液注入容量瓶
- D、容量瓶使用前用蒸馏水洗过
正确答案:B,C
第5题:
用同一NaOH溶液,分别与相同体积的盐酸、醋酸溶液反应,完全反应后消耗了相同量的NaOH溶液.由此说明该盐酸和醋酸溶液的关系是( )
A.H+浓度相同
B.物质的量浓度相同
C.溶质的质量分数相同
D.pH相同
B.物质的量浓度相同
C.溶质的质量分数相同
D.pH相同
答案:B
解析:
【解题指要】 (1)首先应明确盐酸、醋酸溶液分别与NaOH溶液反应,消耗NaOH溶液的量与盐酸、醋酸溶液中所含溶质的量成正比. 从反应方程式中可知它们的质量比和物质的量之比.

由此可知,若消耗NaOH溶液的量相等,则盐酸、醋酸溶液中所含溶质的物质的量一定相等,但质量一定不等,即n(HCl)=n(CH3COOH),m(HCl)≠m(CH3COOH).

质的量浓度相等.故B选项正确.
因不知溶液的总质量,所以溶质的质量分数一般不同,即C选项错误.
(2)其次,应知道盐酸是强酸,醋酸是弱酸,它们的电离程度不同.
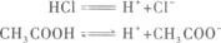
当HCl、CH3COOH的物质的量相同时,溶液中H+的物质的量一定不同,即H+的物质的量浓度一定不同.所以A选项错误.
(3)根据pH=-lg c(H+)可知,H+浓度不同,溶液的pH也一定不同,即溶液的酸性强弱不同.所以D选项也错误.

由此可知,若消耗NaOH溶液的量相等,则盐酸、醋酸溶液中所含溶质的物质的量一定相等,但质量一定不等,即n(HCl)=n(CH3COOH),m(HCl)≠m(CH3COOH).

质的量浓度相等.故B选项正确.
因不知溶液的总质量,所以溶质的质量分数一般不同,即C选项错误.
(2)其次,应知道盐酸是强酸,醋酸是弱酸,它们的电离程度不同.
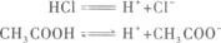
当HCl、CH3COOH的物质的量相同时,溶液中H+的物质的量一定不同,即H+的物质的量浓度一定不同.所以A选项错误.
(3)根据pH=-lg c(H+)可知,H+浓度不同,溶液的pH也一定不同,即溶液的酸性强弱不同.所以D选项也错误.
第6题:
已知某标准NaOH溶液在保存中吸收了少量CO2,用此溶液来标定盐酸溶液,若以甲基橙作指示剂,则使盐酸溶液的浓度标定结果()。
A、偏低;
B、偏高;
C、无影响;
D、无法确定。
参考答案: C
第7题:
称取邻苯二甲酸氢钾(KHP)基准物质0.6306g,标定NaOH溶液。以酚酞为指示剂滴定至终点,用去此溶液29.56mL,求NaOH物质的量浓度。
正确答案:


第8题:
饱和NaOH溶液的NaOH含量约为52%,密度为1.56cm3。求其物质量的浓度?若配置0.1mol/LNaOH溶液1L,应取饱和NaOH溶液多少?
参考答案:饱和NaOH溶液的物质的量的浓度为
=(1.56×1000×52%)÷(40×1)
=20(mol/L)
欲配制1000mL0.1mol/LNaOH需取饱和NaOH溶液的毫升数为:1000×0.1÷20=5(mL)
NaOH物质的量的浓度为20mol/L;配制1000mL0.1mol/LNaOH需取饱和NaOH溶液5mL。
=(1.56×1000×52%)÷(40×1)
=20(mol/L)
欲配制1000mL0.1mol/LNaOH需取饱和NaOH溶液的毫升数为:1000×0.1÷20=5(mL)
NaOH物质的量的浓度为20mol/L;配制1000mL0.1mol/LNaOH需取饱和NaOH溶液5mL。
第9题:
用V1=38.4mL(H+),c1=0.15mol/L的硫酸溶液中和V2=20mL的NaOH溶液,求此NaOH溶液的物质的量的浓度c2?
正确答案: 根据公式c1V1=c2V2,得
c2=0.15×38.4/20=0.29(mol/L)
第10题:
称取NaOH固体4.0g,配成1000mL水溶液,这时NaOH溶液物质的量浓度是()。
- A、0.4%
- B、0.1mol/mL
- C、0.1mol/L
- D、0.01mol/L
正确答案:C
