判断题1%淀粉溶液可按如下步骤配制,称取.1.0g可溶性淀粉后,用刚煮沸的水冲稀至100ml。A 对B 错
题目
对
错
相似问题和答案
第1题:
取葡萄糖1.0g,加水10ml溶解后,加碘试液1滴,该试验若显蓝色,则证明( )。
A.有亚硫酸盐
B.有可溶性淀粉
C.溶液显碱性
D.溶液显酸性
E.有氯化物
第2题:
称取1.0g酚酞,溶于乙醇,用乙醇稀至100ml,该酚酞溶液的浓度为1%。
此题为判断题(对,错)。
第3题:
(5分)准确称取0.2017 g维生素C(C6H806)试样,加入新煮沸的冷蒸馏水l00.0 mL和稀HAc l0.0 mL.以淀粉作指示剂,用0.050 00 mol·L-1的I2标准溶液滴定至终点.用去20.53 mL。计算试样中C6H8O6的质量分数。已知:M(C6H806)=176.1g·mol-1。
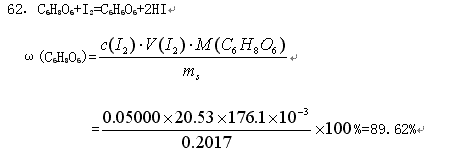
第4题:
饲料级碘化钾中碘离子鉴别试验为:称取0.5g试样,称准至0.01g,置于50ml烧杯中,用于5ml水溶解,加1ml淀粉溶液产生()。
正确答案:蓝紫色
第5题:
精密称取维生素C约0.2g,加新煮沸放冷的蒸馏水100ml,与稀醋酸10ml使溶解,加淀粉指示剂1ml,立即用碘滴定液(0.1mol/L)滴定至溶液显持续的蓝色。此操作中加新煮沸放冷的蒸馏水的目的是()
A使维生素C溶解
B除去水中微生物的影响
C使终点敏锐
D除去水中二氧化碳的影响
E消除水中溶解氧的影响
E
略
第6题:
配制氢氧化钠标准溶液,要求
A.临用新配,用新沸放冷的水溶解
B.先配成饱和溶液,静置数日后,取上清液适量,用新沸放冷的水稀释至所需浓度
C.为消除氢氧化钠中可能含有的少量Na2CO3,配制时需加少量HCl
D.标准液配制后应过滤
E.氢氧化钠加水溶解后需加热煮沸1小时,以除去Na2CO3
第7题:
某注射用药液的配制方法如下:
(1)把1.0g药品溶于水配制成4.0mL溶液a;
(2)取0.1mL溶液a,加水稀释至1.0mL,得到溶液b;
(3)取0.1mL溶液b,加水稀释至1.0mL,得到溶液c;
(4)取0.2mL溶液c,加水稀释至1.0mL,得到溶液d。
由于在整个配制过程中药液很稀,其密度可近似看作1g/cm³。试求:
(1)最终得到的药液(溶液d)中溶质的质量分数;
(2)1.0g该药品可配制溶液d的体积是多少?
分析:溶质的质量分数=溶质的质量/溶液的质量×100%,并利用稀释前后溶质的质量不会改变的知识解决,分步求出各部得到的溶液的溶质质量分数,溶液体积=溶液质量/溶液密度即可.
因为溶液的密度是1g/cm3,所以可直接看成毫升数即是物质的克数,然后利用溶质的质量分数=溶质的质量/溶液的质量×100%计算;
(1)第一步:溶质的质量=1.0g;溶液的质量=4.0mL×1g/cm3=4.0cm3×1g/cm3=4.0g;所以,溶液a中溶质的质量分数=1.0g/4.0g×100%=25%;
溶液b的质量分数=0.1g×25%/1g×100%=2.5%;
溶液c的质量分数=0.1g×2.5%/1g×100%=0.25%;
溶液d的质量分数=0.2g×0.25%/1g×100%=0.05%;
(2)设1.0g药品可配制质量为x的试验针药液,则
1.0g/x×100%=0.05%,
解得x=2000g;由于密度看成1g/mL,所以也就是2000mL;故答案为:(1)0.05%; (2)2000mL.
第8题:
配制该溶液的操作步骤
①计算:▲
②称量:用托盘天平称取所需固体,再用▲mL的量筒量取所需的水;
③溶解:将称得的氯化钾固体放入烧杯中,再倒入量取的水,用玻璃棒充分搅拌;
④装瓶:将配制的溶液倒入试剂瓶,并贴上标签。
50
第9题:
1%淀粉溶液可按如下步骤配制,称取.1.0g可溶性淀粉后,用刚煮沸的水冲稀至100ml。
正确答案:错误
第10题:
配制氢氧化钠标准溶液,要求()
- A、临用新配,用新沸放冷的水溶解
- B、先配成饱和溶液,静置数日后,取上清液适量用新沸放冷的蒸馏水稀释至所需的浓度
- C、为消除氢氧化钠中可能含有的少量Na2CO3,配制时需加少量HCL
- D、标准液配制后应过滤
- E、氢氧化钠加水溶解后需加水煮沸1小时,以除去Na2CO3
正确答案:B
