问答题如下图所示: A为两种元素组成的化合物,B为能使品红溶液褪色的气体,G为红褐色沉淀,试根据图示和题意推断A______、B______、C______、D______、E______、F______、G______.
题目
相似问题和答案
第1题:
(15分)
短周期元素形成的常见非金属固体单质A与常见金属单质B,在加热条件下反应生成化合物C,C与水反应生成白色沉淀D和气体E,D既能溶于强酸,也能溶于强碱。E在足量空气中燃烧产生刺激性气体G,G在大气中能导致酸雨的形成。E被足量氢氧化钠溶液吸收得到无色溶液F。溶液F在空气中长期放置发生反应,生成物之一为H。H与过氧化钠的结构和化学性质相似,其溶液显黄色。
请回答下列问题:
(1)组成单质A的元素位于周期表中第_____________周期,第_________________族。
第2题:
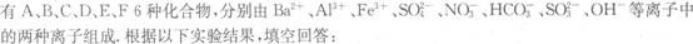
(1)A不溶于水,又不溶于酸.A是__________.
(2)B不溶于水,能溶于酸又能溶于NaOH溶液.B是__________.
(3)C不溶于水,溶于盐酸并放出能使酸性KMn04溶液褪色的无色气体.C是__________.
(4)D溶于水,和盐酸作用放出无色气体,此气体使石灰水浑浊,但不能使KMn04溶液褪色.D是__________.
(5)E溶于水,水溶液显酸性,滴入NaOH溶液时有白色沉淀.E是__________.
(6)F不溶于水,棕褐色,溶于酸所得溶液与SCN-反应呈血红色.F是__________.

第3题:
某气体的水溶液呈酸性,该气体能使酸性高锰酸钾溶液褪色,并能使溴水褪色而出现浑浊,该气体是
A、氯化氢气体
B、硫化氢气体
C、二氧化硫气体
D、二氧化碳气体
E、一氧化碳气体
第4题:
B.氮的非金属性比磷强,则NH3的碱性比PH3强
C.铁、铝在冷的浓硝酸中钝化,铜也能在冷的浓硝酸中钝化
D.S02使品红褪色,加热可恢复红色;S02使溴水褪色,加热也能恢复原色
第5题:

第6题:
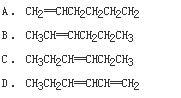

第7题:
 的两种离子组成.它们都易溶于水,用其水溶液做如下实验,实验现象是:
的两种离子组成.它们都易溶于水,用其水溶液做如下实验,实验现象是:
(1)向3种溶液中分别加入盐酸并加热,A溶液与盐酸不反应;B溶液有白色沉淀生成;C
溶液则生成无色无味气体.
(2)向A溶液中加入氢氧化钠溶液,先生成白色沉淀,再继续加氢氧化钠溶液时,沉淀消失.
(3)向C溶液中加入过量氢氧化钠溶液并加热,产生一种有刺激性气味的气体.根据以上现象,可判断A为____________,C为____________
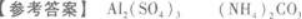 【解题指要】
【解题指要】
(1)向三种溶液中分别加入盐酸并加热.
①B溶液产生白色沉淀,说明B溶液中含有Ag+.易溶于水的银盐只有AgNO3,所以B物质
是AgNO3.

(2)向A溶液中加入NaOH溶液.

所以,A物质是Al2(SO4)3,B物质是AgNO3,C物质是(NH4)2CO3.
第8题:
(5分)有A、B、C、D、E、F六种物质,已知A为一种氯化物,B为一种钠盐,C为一种碱,D为一种常见的气体。它们之间有如下关系:
①A和B的溶液混和无明显现象;
②B和C的溶液混和生成不溶于稀硝酸的白色沉淀E;
③A和C的溶液混和有蓝色沉淀生成;
④把D通入C的溶液中有白色沉淀F生成,该沉淀溶于稀硝酸。
根据上述信息,推断:
(1)写出B、D、F的化学式:B_______;D_______________;F_________________。
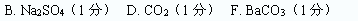
第9题:
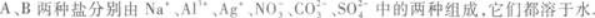
(1)往两种溶液中分别加入盐酸,A溶液不反应,B溶液产生无色无味气体.
(2)往两种溶液中分别加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,B溶液与NaOH不反应.
(3)往两种盐溶液中分别加入BaCl2溶液,都产生白色沉淀.再分别加入稀HNO3,A中沉淀不消失,B中沉淀消失.由此可知,A的化学式为____________,B的化学式为____________.
(1)加入盐酸,B溶液产生无色无味气体.在给出的6种离子中只

即B一定是碳酸盐.
(2)加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,显然这是Al3+的特征反应.其反应方程式为

即A中一定含有Al3+,是铝盐.
(3)向A、B溶液中分别加入BaCl2溶液,都有白色沉淀生成.再分别加入稀HNO3,A中沉淀

第10题:
B.氮的非金属性比磷强,则NH3的碱性比PH3强
C.铁、铝在冷的浓硝酸中钝化,铜也能在冷的浓硝酸中钝化
D.S02使品红溶液褪色,加热可使其恢复红色;S02使溴水褪色,加热也能恢复原色
