NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?
题目
NaCl与KBr各1mol溶于水中所得的溶液与NaBr及KCl各1mol溶于水中所得溶液是否相同?如将CH4及CCl4各1mol混在一起,与CHCl3及CH3Cl各1mol的混合物是否相同?为什么?
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
下列试剂能鉴别NaCl、NaBr、Nal三瓶无色溶液的是( )
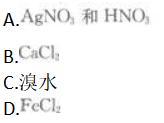
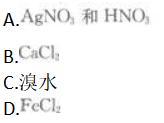
答案:A
解析:
第2题:
等重的葡萄糖及甘油分别溶于100g水中,所得溶液的凝固点、沸点、渗透压是否相同,为什么?
正确答案:不相同。难挥发非电解质溶液的凝固点、沸点、渗透压的计算均与溶质的质量摩尔浓度m有关,等质量的葡萄糖与甘油,其物质的量并不相等,所以引起的溶液依数性性质变化不相同。
第3题:
向含有NaBr、KI的溶液中通入过量的Cl2,然后将溶液蒸干,再灼烧其残渣,最后得到的固体物质是()
A.KCl和I2
B.KCl和NaCl
C.NaCl和KBr
D.KCl、NaCl和I2
参考答案:B
第4题:
下列物质中,何者熔点最低? NaCl KBr KCl MgO
正确答案: KBr熔点最低(因为阴阳离子的半径均大,晶格能小)
第5题:
PH计的甘汞电极通常以()作盐桥。
- A、汞
- B、甘汞溶液
- C、饱和NaCl溶液
- D、饱和KCl溶液
正确答案:D
第6题:
测电导池常数所用的标准溶液是( )。
A.饱和KCl溶液
B.0.01mol/L KCl溶液
C.0.1mol/L NaCl溶液
D.饱和碘溶液
E.纯水
B.0.01mol/L KCl溶液
C.0.1mol/L NaCl溶液
D.饱和碘溶液
E.纯水
答案:B
解析:
第7题:
以下哪种物质不会灼伤皮肤()
- A、强碱、强酸
- B、强氧化剂
- C、溴
- D、KBr、NaBr水溶液
正确答案:D
第8题:
下列物质熔点变化顺序中,不正确的是( )。
A.NaF>NaCl>NaBr>NaI
B.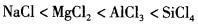
C.LiF>NaCl>KBr>CsI
D.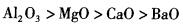
B.
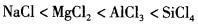
C.LiF>NaCl>KBr>CsI
D.
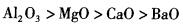
答案:B
解析:
对于离子晶体,半径越小,电荷越多,晶格能越大,熔点越高,在电荷相同时,离子半径越小,离子键越稳定,熔点越高,同一周期自左向右半径逐渐减少,同一主族自上而下半径逐渐增大。
第9题:
有一白色沉淀,加入2mol氨水水沉淀溶解,再加KBr溶液即析出浅黄色沉淀,此沉淀可溶于Na2S2O3溶液中,再加入KI溶液又见黄色沉淀,此沉淀溶于KCN溶液中,最后加入Na2S溶液时析出黑色沉淀.问: (1)白色沉淀为何物? (2)写出各步反应方程式。
正确答案:(1)白色沉淀为AgCl
(2)各步反应为:AgCl+2NH3=[Ag(NH3)2]Cl
Ag(NH3)2Cl+KBr=AgBr↓+KCl+2NH3
AgBr+2Na2S2O3=Na3[Ag(S2O3)2]+NaBr
Na3[Ag(S2O3)2]+KI=AgI↓+Na2S2O3+KNaS2O3
AgI+2KCN=K[Ag(CN)2]+Ki
2K[Ag(CN)2]+Na2S=Ag2S↓+2KCN+2NaCN
第10题:
有KCl和KBr的混合物3.87克,溶于水配成溶液,向溶液中加入足量的AgNO3溶液,产生沉淀,经过滤干燥得6.63克沉淀,则混合物中钾元素的质量分数是多少?(AgBr不溶于水)
正确答案: 因为 K———Ag Δm
39 109 69克
X (6.63—3.87)克
X=1.56克
钾元素的质量分数为:1.56克/3.87克=40.3%
