已知KA(HA)=1.0×10-7,在0.1mol/LHA溶液中,pH值为()A、7.0B、6.0C、8.0D、4.0
题目
已知KA(HA)=1.0×10-7,在0.1mol/LHA溶液中,pH值为()
- A、7.0
- B、6.0
- C、8.0
- D、4.0
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
0.1mol/lNa2CO3溶液的PH值()。(Ka1=4.2*10-7、Ka2=5.6*10-11)
A.10.63
B.5.63
C.11.63
D.12.63
参考答案:C
第2题:
某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶液的PH值为:()?
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
答案:C
解析:因为是弱酸,所以HAc电离能力很弱,HAc浓度近似等于0.1mol/L,由Ka=【H+】*【Ac-】/【HAc】,【H+】和【Ac-】近似相等,可得【H+】=10-3,PH=-lg(氢离子浓度)所以PH值=3
第3题:
已知KA(HA)=1.0×10-7,在0.1mol/LHA溶液中,pH值为()
A.7.0
B.6.0
C.8.0
D.4.0
参考答案:D
第4题:
把NaAc晶体加到0.1mol/LHAc溶液中,将会有下列中哪种变化()?
- A、溶液pH值升高
- B、溶液pH值下降
- C、Ka增加
- D、Ka减小
正确答案:A
第5题:
把NaAc晶体加到0.1mol/L HAc溶液中,将会有下列中哪种变化?
A.溶液pH值升髙
B.溶液pH值下降
C. Ka增加
D. Ka减小
B.溶液pH值下降
C. Ka增加
D. Ka减小
答案:A
解析:
提示:Ka只与温度有关。HAc溶液中加入NaAc使HAc的电离平衡向左移动,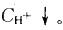
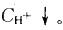
第6题:
0.1mol/l三氯乙酸溶液的PH值为()。(已知Ka=0.23)
A.0.82
B.1.12
C.0.10
D.1.00
参考答案:B
第7题:
当某二元弱酸酸式盐NaHA的浓度为0.lOmol/L时其溶液的pH值为8.31,己知HA的Kal=4.2×10-7,Ka2=5.6×10-11。()
此题为判断题(对,错)。
参考答案:正确
第8题:
某弱酸HA的Ka=1.0x10-3,1.0mol/L的该酸水溶液的pH为( )
A、3.0
B、2.0
C、1.5
D、6.0
参考答案:C
第9题:
在100mL 0.1mol/L苯甲酸溶液中加入10ml 1.0mol/L的HCl,溶液中保持不变的是( )。
A.解离度 B. pH值 C.苯甲酸的浓度 D.苯甲酸的Ka
A.解离度 B. pH值 C.苯甲酸的浓度 D.苯甲酸的Ka
答案:D
解析:
提示:苯甲酸在溶液中存在解离平衡,C6H5COOH=C6H5COO-+H+,加入HCl, 增加H+浓度,平衡向左移动,解离度降低,苯甲酸分子浓度增大,但苯甲酸的解离常数Ka只与温度有关,不随浓度而变。
第10题:
0.1mol•L-1HA溶液(Ka=1.0×10-5)的pH为()
- A、2.0
- B、2.5
- C、3.0
- D、4.0
正确答案:C
