在配合物中,中心原子的杂化轨道类型属内轨型是()。A、sp3d2B、d2sp3C、spD、sp3
题目
在配合物中,中心原子的杂化轨道类型属内轨型是()。
- A、sp3d2
- B、d2sp3
- C、sp
- D、sp3
如果没有搜索结果,请直接 联系老师 获取答案。
如果没有搜索结果,请直接 联系老师 获取答案。
相似问题和答案
第1题:
下列各种说法中正确的是?
A.凡是中心原子采用sp3杂化轨道成键后形成的分子,其空间构型都是正四面体
B.凡AB3型的共价化合物,其中心原子均采用sp2杂化轨道成键
C.在AB2型的共价化合物中,中心原子均采用sp杂化轨道成键
D. sp3杂化可分等性sp3杂化和不等性sp3杂化
A.凡是中心原子采用sp3杂化轨道成键后形成的分子,其空间构型都是正四面体
B.凡AB3型的共价化合物,其中心原子均采用sp2杂化轨道成键
C.在AB2型的共价化合物中,中心原子均采用sp杂化轨道成键
D. sp3杂化可分等性sp3杂化和不等性sp3杂化
答案:D
解析:
提示:通过sp杂化后形成的分子为直线;通过sp2杂化后形成的分子为正三角形,也有V字形的;通过SP3杂化后形成的分子有正四面体、三角锥形,还有V字形。
第2题:
关于原子轨道的说法正确的是()
- A、凡中心原子采取sp3杂化轨道成键的分子其几何构型都是正四面体.
- B、CH4分子中的sp3杂化轨道是由4个H原子的1s轨道和C原子的2p轨道混合起来而形成的;
- C、sp3杂化轨道是由同一原子中能量相近的s轨道和p轨道混合起来形成的一组能量相等的新轨道;
- D、凡AB3型的共价化合物,其中心原子A均采用sp3杂化轨道成键.
正确答案:C
第3题:
②在生成物中,A的晶体类型为________,含极性共价键的分子的中心原子轨道杂化类型为_________。
正确答案:
离子晶体; SP
离子晶体; SP
第4题:
27元素Co的[Co(NH3)6]3+是内轨型配合物,则中心离子未成对电子数和杂化轨道类型是()
- A、4,sp3d2
- B、0,sp3d2
- C、4,d2sp3
- D、0,d2sp3
正确答案:D
第5题:
价键理论认为,决定配合物空间构型主要是()。
- A、配体对中心离子的影响与作用
- B、中心离子对配体的影响与作用
- C、中心离子(或原子)的原子轨道杂化
- D、配体中配位原子对中心原子的作用
正确答案:C
第6题:
形成外轨型配合物时,中心原子不可能采取的杂化方式是()
- A、d2sp3
- B、sp3
- C、sp
- D、sp3d2
- E、sp3d
正确答案:A
第7题:
已知配离子[28Ni(H2O)4]2+为顺磁性物质,则该配离子是()
- A、内轨配合物,dsp2杂化
- B、外轨形配合物,sp3杂化
- C、外轨形配合物,sp3d2杂化
- D、内轨配合物,d2sp3杂化
正确答案:B
第8题:
在下列物质的分子中,中心原子采用sp杂化轨道成键,分子空间构型是直线型的是( )。
A.
B.
C.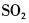
D.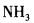

B.

C.
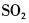
D.
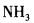
答案:A
解析:
见杂化轨道类型。中心原子Be采用sp杂化与Cl原子成键。
第9题:
凡是配位数为4的分子,其中心原子均采用sp3杂化轨道成键。
正确答案:错误
第10题:
内轨型配合物和外轨型配合物的区别在于:内轨型配合物中,中心离子使用内层电子形成配位键;而外轨型配合物中,中心离子是使用外层电子形成配位键。
正确答案:错误
