反应C(s)+H2O(g)=CO(g)+H2(g) ΔrHθm>0,下列叙述正确的是()A、此反应为吸热反应,升高温度则正反应速率增加,逆反应速率减少,所以平衡右移B、增大压力不利于H2O(g)的转化C、升高温度使其Kθ减少D、加入催化剂可以提高反应物的转化率
题目
反应C(s)+H2O(g)=CO(g)+H2(g) ΔrHθm>0,下列叙述正确的是()
- A、此反应为吸热反应,升高温度则正反应速率增加,逆反应速率减少,所以平衡右移
- B、增大压力不利于H2O(g)的转化
- C、升高温度使其Kθ减少
- D、加入催化剂可以提高反应物的转化率
相似问题和答案
第1题:
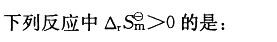
B.H2(g)+3H2(g)→2NH3(g)
C. NH4Cl(s)→NH3(g)+HCl(g)
D.CO2(g)+2NaOH(aq)→Na2CO3(aq) +H2O(l)
第2题:
已知反应C(s) + 2H2O(g) ←→ CO2(g) + 2H2(g) 的Kp为A,用A 表示下列各反应的平衡常数KpCO2(g)+2Hg)←C(s)+ 2H2O(g)Kp=()
正确答案:1/A
第3题:
A、5
B、4
C、3
D、2
第4题:
已知反应C(s) + 2H2O(g) ←→ CO2(g) + 2H2(g) 的Kp为A,用A 表示下列各反应的平衡常数Kp2C(s)+4H2O(g) ←→ 2CO2(g) + 4H2(g) Kp=()
正确答案:A2
第5题:
已知在一定温度下: SnO2(s)+2H2(g) === Sn(s)+2H2O(g) KΘ1=21.0 CO(g)+H2O(g) === CO2(g)+H2(g) KΘ2=0.034 因此,下列反应SnO2(s)+2CO(g) === Sn(s)+2CO2(g)的3KΘ3=()
- A、21.0
- B、0.714
- C、0.0243
- D、21.6
正确答案:C
第6题:
B.2CH4(g)+4O2(g)===2CO2(g)+4H2O(L)
C.CH4(g)+2O2(g)===CO2(g)+2H2O(g)
D.2CH4(g)+4O2(g)===2CO2(g)+4H2O(g)
第7题:
对于反应:C(S)+H2O(g)⇄CO(g)+H2(g),△H>0,为了提高C(S)的转化率,可采取的措施是()
- A、多加入C(S)
- B、降低反应温度
- C、增大体系的总压力
- D、增大H2O(g)的分压
正确答案:D
第8题:
下列反应中表达式正确的是。
A、Na(s)+1/2Cl2(g)=NaCl(s)ΔrHmθ=ΔfHmθ(NaCl,s)
B、C(石墨)+H2(g)=1/2C2H4(g)ΔrHmθ=ΔfHmθ(C2H4,g)
C、CO(g)+1/2O2(g)=CO2(g)ΔrHmθ=ΔfHmθ(CO2,g)
D、CH3OH(g)+O2(g)=CO(g)+2H2O(g)ΔrHmθ=ΔcHmθ(CH3OH,g)
第9题:
下列反应方程式中哪个反应放出的热量最多()
- A、CH(g)+2O2(g)CO2(g)+2H2O(l)
- B、2CH(g)+4O2(g)2CO2(g)+4H2O(l)
- C、CH(g)+2O2(g)CO2(g)+2H2O(g)
- D、2CH(g)+4O2(g)2CO2(g)+4H2O(g)
正确答案:B
第10题:
已知反应C(s) + 2H2O(g) ←→ CO2(g) + 2H2(g) 的Kp为A,用A 表示下列各反应的平衡常数Kp 1/2C(s)+ H2O(g) ←→ 1/2CO2(g) + H2(g) Kp=()
正确答案:A1∕2
