在0.01mol/L硫酸溶液中,水电离出的[H+]()。A、0.02mol/LB、1×10-7mol/LC、5×10-13mol/LD、1×10-12mol/L
题目
在0.01mol/L硫酸溶液中,水电离出的[H+]()。
- A、0.02mol/L
- B、1×10-7mol/L
- C、5×10-13mol/L
- D、1×10-12mol/L
相似问题和答案
第1题:
有下列水溶液:(1)0.01mol·L-1CH3COOH(2)0.01mol·L-1CH3COOH溶液和等体积0.01mol·L-1HCl溶液混合(3)0.01mol·L-1CH3COOH溶液和等体积0.01mol·L-1NaOH溶液混合(4)0.01mol·L-1CH3COOH溶液和等体积0.01mol·L-1NaAc溶液混合则它们的pH值由大到小的正确次序是()
A、(1)(2)(3)(4)
B、(1)(3)(2)(4)
C、(4)(3)(2)(1)
D、(3)(4)(1)(2)
第2题:
A. S0>S1>S2>S3 B. S0>S2>S1>S3 C. S0>S1>S2=S3 D. S0>S2>S3>S1
第3题:
酸性染料是
A、在溶液中能电离出阴离子的染料
B、含有酸性发色团的染料
C、溶液呈酸性的染料
D、溶液呈碱性的染料
E、在溶液中能电离出阳离子的染料
第4题:
1升溶液中含硫酸4.904克,此溶液的物质的量浓度C(1/2H2SO4)是()。
- A、0.05mol/Lmg/L
- B、0.5mol/L
- C、0.1mol/Lmol/L
- D、0.01mol/L%
正确答案:C
第5题:
H2SO4在水溶液中()。
- A、电离度很大,酸度也很大
- B、氢全部电离出,酸度也很大
- C、电离度很大,酸性也很强
- D、氢全部电离出,酸性也很强
正确答案:C
第6题:
B.物质的量浓度相等的H2S和NaHS混合溶液中:
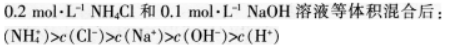
C.
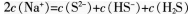
D.将①0.01mol·L-1的CH3COOH溶液;②0.01mol·L-1的盐酸;③pH=12的氨水;④pH=12的NaOH溶液稀释相同倍数后溶液的pH:③>④>②>①
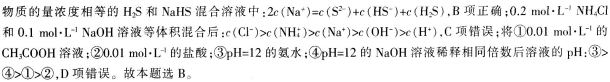
第7题:
有下列溶液: ①0.01mol·L-1HAc溶液; ②0.01mol·L-1HAc与等体积等浓度的NaOH溶液混合; ③0.01mol·L-1HAc与等体积等浓度的HCl溶液混合; ④0.01mol·L-1HAc与等体积等浓度的NaAc溶液混合。 其pH值排列顺序正确的是()。
- A、①>②>③>④
- B、①>③>②>④
- C、④>③>②>①
- D、②>④>①>③
正确答案:D
第8题:
已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A.该溶液的pH=4
B.升高温度,溶液的pH增大
C.此酸的电离平衡常数约为1×10-7
D.由HA电离出的c(H+)约为水电离出的c(H+)的106倍
第9题:
硫酸铜测定时采用的硫代硫酸钠标准滴定溶液的浓度为()。
- A、0.01mol/L
- B、0.05mol/L
- C、0.10mol/L
- D、0.20mol/L
正确答案:C
第10题:
22℃时,在0.01mol/L的HCl溶液中,[H+]=10-2mol/L,则[OH-]=()mol/L。
- A、0
- B、10-12
- C、10-7
- D、10-2
正确答案:B
