单选题0.050mol/LNaAc溶液的pH值为(Ka=1.8×10-5)()。A 3.02B 10.98C 8.72D 8.87
题目
3.02
10.98
8.72
8.87
相似问题和答案
第1题:
A.3.02
B.10.98
C.8.72
D.8.87
第2题:
A.2.7
B.2.72
C.2.722
D.5.44
第3题:
A、NaAc溶液(Ka=1.76×10-5)
B、NH₃H₂O溶液(Kb=1.78×10-5)
C、K₂S溶液(K₂=7.1×10-15)
D、HCN溶液(Ka=4.0×10-10)
第4题:
已知Hac的离解常数为1.8×10-5,则5.0×10-5mol/LHAc与5.0×10-2mol/LNaAc混合溶液的PH值为()。
- A、9.26
- B、7.74
- C、8.76
- D、9.86
正确答案:B
第5题:
A. 6:1 B. 4:1 C. 5:1 D. 10:1
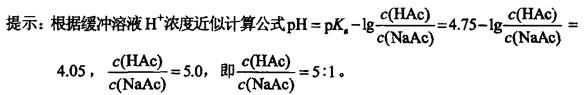
第6题:
A.2.9
B.2.87
C.2.75
D.5.7
第7题:
某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶液的PH值为:()?
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
答案:C
解析:因为是弱酸,所以HAc电离能力很弱,HAc浓度近似等于0.1mol/L,由Ka=【H+】*【Ac-】/【HAc】,【H+】和【Ac-】近似相等,可得【H+】=10-3,PH=-lg(氢离子浓度)所以PH值=3
第8题:
A.5.13
B.2.87
C.5.74
D.4.88
第9题:
在HAc-NaAc的混合液中,HAc和NaAc的浓度都为0.1mol/L,HAc的Ka=1.8×10-5。此缓冲溶液的pH值为()。
A4.74
B7.56
C8.86
D9.26
A
略
第10题:
已知氨水中的氨浓度为0.500mol/L,求溶液的pH值(Kb=1.8×10-5)
正确答案: 可应用近似公式求解
=3.0×10-3(mol/L)
pOH=-lg[OH-]=2.52
pH=14.00-pOH=11.48
