单选题除去FeCl3溶液中混有的FeCl2,可向溶液中( ).A 加入CuB 加入FeC 通入适量Cl2D 通入过量H2S
题目
加入Cu
加入Fe
通入适量Cl2
通入过量H2S
相似问题和答案
第1题:
下列除去杂质的方法正确的是
A.除去CO2中混有的CO:用澄清石灰水洗气
B.除去BaCO3固体中混有的BaSO4:加过量盐酸后,过滤、洗涤
C.除去FeCl2溶液中混有的FeCl3:加入过量铁粉,过滤
D.除去Cu粉中混有的CuO:加适量稀硝酸后,过滤、洗涤
CO2可以被澄清石灰水吸收,而CO不可以,故A项错。盐酸可以将BaCO3反应除去,而不能溶解BaSO4,故B项错;C项,2FeCl3 + Fe = 3FeCl2,过量的铁过滤,即可除去,正确;Cu和CuO均可以被HNO3溶解,故D项错。
第2题:
A、水溶液>混悬液>胶囊剂>散剂
B、水溶液>混悬剂>散剂>胶囊剂
C、散剂>胶囊剂>片剂>水溶液
D、水溶液>混悬液>片剂>胶囊剂
E、水溶液>胶囊剂>混悬液>片剂
第3题:
蒸发操作中除去的是溶液中的溶质。()
第4题:
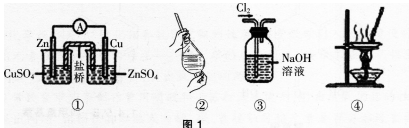
B.可用装置②进行CCl4萃取碘水中碘的实验
C.可用装置③除去Cl2中含有的少量HCl
D.可用装置④蒸干FeCl3饱和溶液制备FeCl3晶体
第5题:
B.铁粉
C.氯气
D.氢氧化钠
第6题:
下列实验设计和结论相符的是
A.将碘水倒入分液漏斗,加适量乙醇,振荡后静置,可将碘萃取到乙醇中
B.某气体能使湿润的红色石蕊试纸变蓝,该气体水溶液一定显碱性
C.某无色溶液中加Ba(NO3)2溶液,再加入稀盐酸,沉淀不溶解,则原溶液中一定有SO42-
D.在含FeCl2杂质的FeCl3溶液中通足量Cl2后,充分加热,除去过量的Cl2,即可得到较纯净的FeCl3溶液
B【解析】A项,乙醇不可以作为萃取剂,错;B项,石蕊变蓝,则肯定为碱性,正确。C项,若原溶液中含有SO32 -,生成BaSO3,再加入HCl,则与溶液的NO3- 结合,相当于HNO3,则可以氧化BaSO3至BaSO4,沉淀不溶解,故错;D项,加热时,FeCl3会水解,错。
第7题:
A. 浓硫酸
B. 氢氧化钠溶液
C. 饱和碳酸氢钠溶液
D. 饱和NaHSO3溶液
第8题:
A. FeCl3>FeCl2>KCl>CACl2
B. FeCl3>KCl>FeCl2>CACl2
C. FeCl3>FeCl2>CACl2>KCl
D. >CACl2>KCl>FeCl3>FeCl2
第9题:
B.过量铁粉与CuCl2溶液
C.过量氯水与FeCl2溶液
D.过量铁粉与FeCl3溶液

Fe3+.所以只要有Fe3+生成,加入KSCN溶液后就能显示血红色.这与氯水过量与否关系不大,只是若氯水过量,可将FeCl2全部变成FeCl3.而与KSCN反应显示血红色,不必全部转化成FeCl3.所以,C选项为正确选项.
第10题:
当盐酸溶液中FeCL2达到饱和值时酸洗时间()
- A、很短
- B、无变化
- C、很长
正确答案:C
