评价生物等效性的药动学参数有:A.AUC B.Cl C.t D.k E.C
题目
B.Cl
C.t
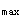
D.k
E.C
参考答案和解析
生物等效性(bioequivalence,BE)是指一种药物的不同制剂在相同试验条件下,给以相同剂量,反映其吸收程度和速度的主要药动学参数无统计学差异。通常意义的生物等效性研究是指采用生物利用度的研究方法,以药动学参数为指标,根据预先确定的等效标准和限度进行的比较研究,评价同种药物不同制剂内在质量是否相等。
生物等效性评价是对求得的生物利用度参数进行统计分析,血药浓度法的评价参数是AUC、C
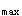 、t
、t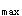 。正确答案为ACE。
。正确答案为ACE。相似问题和答案
第1题:
用统计矩法可求出的药动学参数有
A.K, Vm
B.Km, , V
C.Cmax
D.tmax
E.a
第2题:
A、群体药动学研究的目的是为个体化给药提供依据
B、群体药动学可用于生物利用度研究
C、群体药动学研究血药浓度在个体间的变异性
D、群体药动学研究病人个体特征和药动学参数之间的关系
E、群体药动学将经典药动学与药效学结合起来
第3题:
A、与原研药药学等效
B、与原研药生物等效
C、与原研药含量等效
D、与原研药药学等效且生物等效
E、与原研药药物经济学相当
第4题:
制剂的生物利用度研究属于
A.药效学评价
B.药动学评价
C.药剂学评价
D.临床疗效评价
E.经济学评价
解析:药物药剂学评价的主要内容是研究影响制剂生物利用度的主要因素。
第5题:
以药动学参数为指标,比较同一种药物相同或者不同剂型的制剂,在相同的试验条件下,其活性成分吸收程度和速度有无统计学差异的人体试验是
A、Ⅰ期临床试验
B、Ⅱ期临床试验
C、Ⅲ期临床试验
D、Ⅳ期临床试验
E、生物等效性试验
第6题:
治疗药物的有效性评价不包括( )。
A.理化参数评价
B.药效学评价
C.药剂学评价
D.药动学评价
E.临床疗效评价
第7题:
一种药物不同剂型在相同试验条件下,给相同剂量药物,其吸收程度和速度的主要药动学参数无统计学差异
A.蓄积
B.第二相反应
C.药物相互作用
D.生物等效性
E.酶抑制作用
第8题:
用于评价制剂生物等效性的药物动力学参数有
A、生物半衰期(t+1/2)
B、清除率(CI)
C、血药峰浓度(Cmax)
D、表现分布容积(V)
E、血药浓度-时间曲线下面积(AUC)
暂无解析,请参考用户分享笔记
第9题:
新药的临床前研究包括的内容是
A、生物等效性试验
B、制备工艺、理化性质、质量标准、药理、毒理、动物药动学等研究
C、不良反应的考察
D、人体安全性评价
E、科研文章
第10题:
符合新药报批人体生物利用度实验要求的叙述为
A.生物利用度的计算结果只能由血药浓度得到
B.不能用代谢产物求算生物利用度
C.缓控释制剂的药动学参数除一般的外,还应提供可以描述缓控释制剂特殊释放行为的动力学参数
D.生物等效性评价采用双单侧检验,对AUC和Cmax直接进行统计分析
E.若受试制剂的AUC的95%.的可信限在标准参比制剂的95%.~105%.的范围内,可以认为两种制剂生物等效
